SPIOs und der potenzielle Einsatz als Tracer in der MPI-Bildgebung
Superparamagnetische Eisenoxid-Nanopartikel (engl. Superparamagnetic Iron Oxide, SPIOs) haben ein großes diagnostisches Potential und können als Tracer zur Darstellung von Gefäßen und Organen genutzt werden. Mit der Magnetpartikelbildgebung (engl. Magnetic Particle Imaging, MPI) ist ein Bildgebungsverfahren entwickelt worden, das Partikel direkt und unabhängig vom Gewebehintergrund messen kann.
MPI – eine flexible Bildgebungsmethode mit großem Potential

MPI nutzt ähnlich wie die Magnetresonanztomographie (MRT) Magnetfelder und regt die Partikel durch sowohl örtlich als auch zeitlich variierende Felder an. Die Partikel reagieren mit einer ortsabhängigen Magnetisierungsantwort, die mit Empfangsspulen erfasst werden kann. Das Verfahren wurde 2005 in Hamburg von Bernhard Gleich und Jürgen Weizenecker erstmals vorgestellt, wofür sie 2016 mit dem europäischen Erfinderpreis gewürdigt wurden. MPI ist strahlungsfrei, sehr sensitiv und bietet eine hohe zeitliche Auflösung mit mehr als 40 Volumen pro Sekunde. Zudem ist MPI inhärent dreidimensional und kann das Untersuchungsvolumen flexibel abtasten. In der präklinischen Forschung hat sich bereits gezeigt, dass zahlreiche medizinische Fragestellungen mittels MPI adressiert werden können. Unter anderem zählen hierzu die Detektion ischämischer und hämorrhagischer Schlaganfälle sowie die Darstellung des Gefäßbaums in Echtzeit, was für Gefäßinterventionen in 3D mit Live-Visualisierung interessant sein kann. Um das große Potential der Magnetpartikelbildung allerdings in die klinische Anwendung zu bringen sind künftig zwei Dinge entscheidend: die Entwicklung von MPI-Scannern in humaner Größe und die Verfügbarkeit klinisch nutzbarer SPIOs.
SPIOs – nicht zu klein und nicht zu groß
Grundlage für die klinische Umsetzung von MPI ist die Verfügbarkeit von SPIOs, die für die Anwendung am Menschen zugelassen sind. Viele SPIOs, die bereits als Tracer in der Magnetresonanztomographie (MRT) verwendet werden, verfügen nicht über die magnetischen Eigenschaften, die für die Signalerzeugung in der MPI notwendig sind. Insbesondere haben sie oft nicht die erforderliche Größe. Für MPI ist es entscheidend, dass die Partikel eine nicht-lineare Magnetisierungskurve haben und schon bei moderaten Feldstärken sättigen. Sind die Partikel zu klein, tritt der Sättigungseffekt erst bei großen Feldstärken auf und die Signalqualität ist folglich sehr gering. Sind sie zu groß, können die Partikel nicht mehr schnell genug auf das angelegte Wechselfeld reagieren, sodass auch in diesem Fall kaum Signal erzeugt wird.
Ideal sind Partikel mit einem Kerndurchmesser zwischen 15 und 30 Nanometern und einer ausreichend großen nichtmagnetischen Hülle, die eine Wechselwirkung zwischen den Partikeln verhindert (meist 50 – 80 Nanometer hydrodynamischer Durchmesser). Ein Tracer, der genau in diesen Bereich fällt, ist der Wirkstoff Ferucarbotran. „Ferucarbotran ist ein Glücksgriff für MPI. Dieser bereits in den 2000er Jahren in der MRT genutzte Wirkstoff bietet eine sehr gute MPI-Performance und hat den großen Vorteil, dass er schon klinisch erprobt ist für die Anwendung in der MRT. Erste Messungen bestätigen, dass sich Ferucarbotran sehr gut für die MPI-Bildgebung eignet“, erläutert Tobias Knopp, Professor für Biomedizinische Bildgebung, UKE/TUHH, Hamburg.
Stand der MPI-Technologie
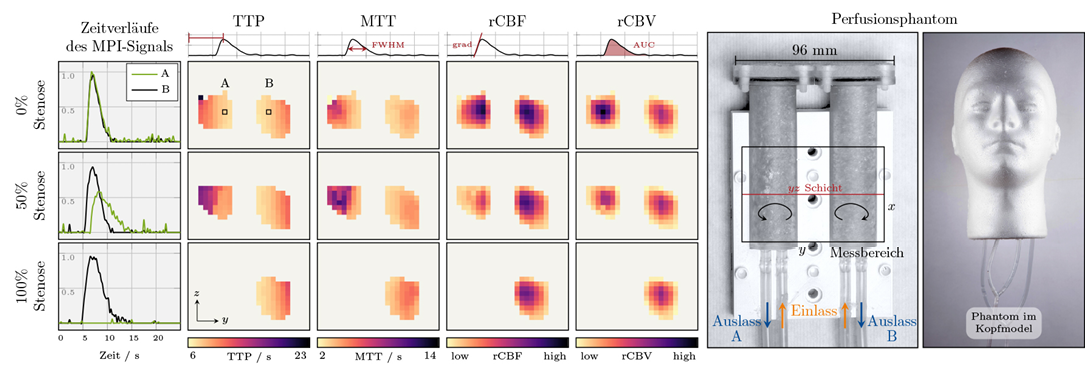
Eine etwaige Zulassung von SPIOs für die MPI ist allerdings kurzfristig nicht absehbar, da diese mit großem Aufwand und hohen Kosten verbunden ist. Aktuell werden MPI-Scanner primär im akademischen Umfeld erforscht und entwickelt. In Deutschland wird zum Beispiel am Brückeninstitut für Biomedizinische Bildgebung (Universitätsklinikum Hamburg-Eppendorf und Technische Universität Hamburg) an der Entwicklung von MPI-Tomographen gearbeitet. So konnte das Team von Tobias Knopp den ersten MPI-Scanner entwickeln, mit dem auch Messungen am menschlichen Kopf möglich sein werden (Abbildung 1). Ähnliche Systeme werden derzeit in China und in den USA geplant. „Auf der jährlich stattfindenden MPI-Konferenz, dem International Workshop on Magnetic Particle Imaging (IWMPI), werden viele Forschungsbeiträge in Richtung humaner MPI-Scanner vorgestellt.“ erläutert Knopp und betont: „Für die großen Medizintechnikhersteller ist jetzt der richtige Zeitpunkt in die Produktentwicklung einzusteigen. Auch wenn es noch weiteres Verbesserungspotential gibt, ist die MPI-Technologie ausgereift und wir wissen, wie man qualitativ hochwertige Tomographen herstellen kann.“ Das Hamburger Forschungsteam konnte in Hirnphantomversuchen bereits zeigen, dass der entwickelte Prototyp Schlaganfälle darstellen kann und sich aus den zeitlich aufgelösten MPI-Volumendaten auch Perfusionsparameterkarten wie der zerebrale Blutfluss oder das zerebrale Blutvolumen ableiten lassen (Abbildung 2). „Wir sind zuversichtlich, dass MPI die Translation aus der Forschung in die Klinik gelingen kann. Unser MPI-Scanner hat gezeigt, dass sich die Technologie auch mit sehr geringem technischem Aufwand realisieren lässt und damit kostengünstig herstellbar wäre. Unser System wird an einer einfachen Steckdose betrieben,“ beschreibt Knopp die Vorzüge des Scanners. Zukünftige MPI-Systeme könnten sogar mobil betrieben werden und eine Nutzung auf der Intensivstation oder vor der Krankenhausaufnahme in speziell ausgerüsteten Rettungswagen ermöglichen.
Profil

Tobias Knopp ist Professor für Biomedizinischee Bildgebung am Universitätsklinikum Hamburg-Eppendorf (UKE) und der Technischen Universität Hamburg (TUHH). Weiterhin leitet er eine Arbeitsgruppe für Data Science und KI an der Fraunhofer-Einrichtung für Individualisierte und Zellbasierte Medizintechnik (IMTE). Er ist Mitorganisator der jährlichen IWMPI und vertritt das International Journal on Magnetic Particle Imaging (IJMPI) als Editor-in-Chief.
